Capilaridad natural de un líquido
Con seguridad ya habrás observado gotas de lluvia en el parabrisas de un automóvil, ya secaste una mesa con un papel o servilleta, ya también habrás preguntado cómo es que hacen las plantas para conseguir introducir los nutrientes desde la raíz hasta sus hojas. Habiendo o no pensado en ello, todas estas preguntas apuntan a un solo concepto físico de la naturaleza, el concepto de capilaridad.
Capilaridad es la subida (o bajada) de un líquido a través de un tubo fino, que recibe el nombre de capilar. Este fenómeno es el resultado de la acción de la interacción de las moléculas de agua con el vidrio (considerando que el tubo por el que el líquido se desplaza es de ese material). Esa interacción depende de algunos parámetros como el diámetro del tubo (cuanto más fino, mayor su adherencia), el tipo de líquido y su viscosidad, que por su parte, depende de la temperatura, cuanto más caliente, es menos viscoso.
Esto se da más o menos de la siguiente forma: Las moléculas del líquido son atraídas por las moléculas del tubo por causa de las interacciones intermoleculares. De esta forma, el líquido queda “pegado” en las paredes.
La acción de la atracción
Lo que logra que ella (el agua) suba es lo siguiente: la molécula del tubo que está inmediatamente por encima de la superficie del líquido atrae al mismo para que comience a subir alineándose a esa molécula que lo atrajo. Cuanto esto sucede, la molécula inmediatamente encima comienza a atraer el líquido y el ciclo se repite.
Seguramente ya viviste un fenómeno de este tipo, pero tal vez no recuerdes o no tengas prestado atención. Haz lo siguiente: derrama un poco de agua sobre una superficie lisa, toma una servilleta de papel y tómala de forma que apenas la punta toque el agua derramada.
Observa como el agua va subiendo hacia la servilleta y el agua de la mesa disminuyendo. Fíjate que el fenómeno de capilaridad no está restringido a los tubos de vidrio, sucede también con otro tipo de experiencias.
Segundo experimento: Derrama un poco más de agua en una superficie lisa solo que esta vez cerca del borde. Sumerge tu dedo en el agua, haz un pequeño camino para que ella escurra por el borde. Fíjate que el agua que va cayendo va “jalando” el agua que está en la superficie hasta disminuirla considerablemente.
Esto no es capilaridad, pero muestra claramente la acción de las fuerzas intermoleculares existentes en el agua, como una molécula logra influenciar las demás. Recuerda que en el agua estas fuerzas son del tipo puentes de hidrógeno, extremadamente fuertes.
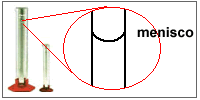
Si ya tuviste la oportunidad de realizar alguna experiencia en laboratorio de química y aprendiste a hacer lectura de volúmenes en probetas, recuerda que existe un menisco, una pequeña curvatura que se forma junto a las paredes de la probeta. Lo que causa ese menisco es la capilaridad.
Un consejo para casa: cuando recibas flores y vayas a colocarlas en un jarrón, sumerge los tallos en el agua y córtalos en un punto que esté sumergido. Esto evita la entrada de aire en los tubos existentes en los tallos que causan la irrupción del flujo de agua que suben por ellos (capilaridad). Si cortas los cabos por un nivel debajo del agua, el flujo se mantendrá y el agua logrará llegar hasta las flores lo cual hará que duren mucho más.
Además de estas experiencias cotidianas, la capilaridad tiene una gran importancia en diversas áreas de la ciencia y la tecnología. En la medicina, por ejemplo, se utiliza en la administración de medicamentos a través de parches transdérmicos. Los medicamentos se disuelven en un líquido que se absorbe a través de la piel gracias a la capilaridad. En la ingeniería, la capilaridad se utiliza en la fabricación de dispositivos microfluídicos, que son sistemas que manipulan pequeñas cantidades de líquidos. Estos dispositivos se utilizan en una variedad de aplicaciones, desde pruebas de diagnóstico médico hasta la fabricación de chips de computadora.
En la naturaleza, la capilaridad juega un papel crucial en la vida de las plantas. Las raíces de las plantas absorben agua del suelo a través de un proceso llamado absorción radicular. Este agua se mueve hacia arriba a través de los tallos de las plantas y llega a las hojas, donde se utiliza en la fotosíntesis. Este movimiento del agua es posible gracias a la capilaridad.
En resumen, la capilaridad es un fenómeno fascinante que se puede observar en nuestra vida diaria y que tiene una gran importancia en diversas áreas de la ciencia y la tecnología. Aunque puede parecer un concepto abstracto, la capilaridad es un fenómeno muy real que tiene un impacto directo en nuestro mundo.