Las membranas y la presión osmótica
En los seres vivos en los seres vivos abundan las membranas. Como veremos en otro momento, el intercambio de materiales con el exterior lo efectúan los seres vivos a través de membranas. Las membranas pueden ser de tres tipos: impermeables, sino permiten el paso a través de ellas de ninguna molécula; permeables, si pueden pasar todas las moléculas; y semi permeables, si sólo permite el paso de algunas moléculas pequeñas pero no de las grandes. De estas últimas vamos a tratar, por ser las más abundantes en los organismos vivos.
Construyamos un aparato como el representado en la figura a continuación:
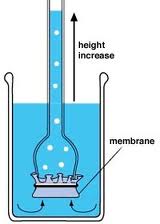
Para ello tomamos un recipiente de vidrio en el que colocamos como fondo una membrana semi permeable. Podemos utilizar un trozo de pergamino. Como prolongación por la parte superior, ajustaremos un tubo también de vidrio. Ahora haremos con la siguiente experiencia:
Se llena al recipiente hasta el comienzo del tubo, con una solución en agua de sal común (NaCl). El recipiente se introduce en otro mayor lleno de agua corriente. Al cabo de algún tiempo observaremos como el nivel del agua va aumentando en el tubo, mientras que desciende en el recipiente mayor. Es decir, parte del agua corriente del recipiente grande ha pasado a través de la membrana al otro recipiente. Esta diferencia de niveles entre ambos recipientes viene determinada por una presión que denominaremos presión osmótica.
Las moléculas de agua pequeñas, penetran fácilmente por los poros de la membrana. Pero las moléculas de la sustancia disuelta de mayor tamaño, no pueden atravesarla. Entonces, habrá más proporción de agua fuera que dentro y al tender a igualarse, el agua sigue pasando de uno a otro recipiente hasta que el peso del agua en el tubo compensa la presión. Se ha llegado entonces al equilibrio.
La presión osmótica de una solución depende de su concentración, es decir del número de moléculas que disueltas independientemente del tamaño de esas moléculas.
No por ser mayores producen más presión. A mayor concentración, mayor presión osmótica. Según esto, el agua pura, sin ninguna sustancia disuelta, presentará una presión osmótica igual a cero.
También depende de la temperatura. La presión osmótica de una solución aumenta con la temperatura. Es decir que mayor temperatura mayor presión osmótica.
Soluciones y hipertónicas, hipotónicas y isotónicas
En general, se produce el fenómeno de ósmosis en los seres vivos cuando hay movimiento de agua de una solución a otra de mayor concentración.
Si se comparan dos soluciones, la de mayor concentración recibe el nombre de hipertónica y la de menor concentración hipotónica. Si las dos tienen la misma concentración, se denominan isotónicas.
Los glóbulos rojos de nuestra sangre están rodeados de una membrana semi permeable. Supresión osmótica es equivalente a la de una solución salina al 7 x 1000. Si se coloca en otra solución más concentrada, pierden líquido y por consiguiente se arrugan.
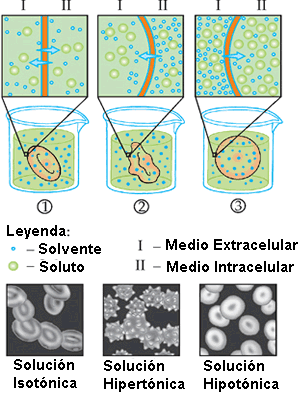
Este fenómeno recibe el nombre de plasmólisis. Cuando se ponen en agua, ésta penetra y los glóbulos rojos se hinchan. A este fenómeno se le llama turgencia. Puede llegar incluso a romperse su membrana, saliendo el contenido al agua, con lo que esta se tiñe de rojo.
