Astrofísica – Leyes de Kirchoff
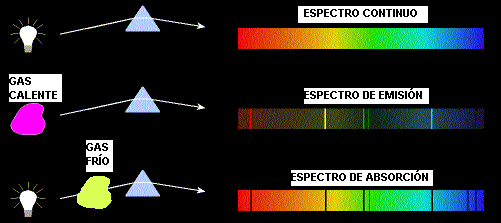
1 – Un cuerpo opaco, caliente, sólido, líquido o gaseoso, emite un espectro continuo
2 – Un gas transparente produce un espectro de líneas brillantes (de emisión). El número y la posición de estas líneas depende de los elementos químicos presentes en el gas.
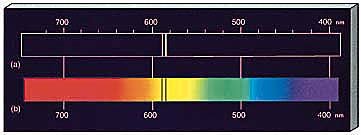
3 – Si un espectro continuo pasa por un gas a temperatura mas baja, el gas frío causa la presencia de líneas oscuras (absorción). El número y la posición de estas líneas depende de los elementos químicos presentes en el gas.
Simulación de Líneas
Independiente de que un átomo aislado solo emita en determinada amplitud de onda, muchos átomos comprimidos juntos en un material, emiten radiación en una banda de líneas ya que tienen velocidades diferentes y los largos de onda se desplazan por el efecto Doppler.
Es importante notar que las líneas oscuras no significan ausencia de luz, solamente el contraste de menos luz. El gas más frío absorbe más radiación que emite y por tanto genera líneas oscuras.
Si estuviese en equilibrio, esto es, ni caliente ni frío, un gas absorbe la radiación que viene en su dirección y la reemite en todas direcciones, causando una disminución de flujo en la dirección de la fuente. Si no hay equilibrio el gas se calienta.
Es crucial entender que las leyes de Kirchoff no solo son relevantes para la astrofísica, sino que también tienen aplicaciones en muchas otras áreas de la física y la ingeniería. Por ejemplo, se utilizan en la termodinámica para analizar los intercambios de calor, en la teoría de circuitos eléctricos para entender cómo fluye la corriente y en la óptica para analizar cómo se propaga la luz.
Además, estas leyes también han jugado un papel crucial en el desarrollo de la teoría cuántica. De hecho, fue la observación de los espectros de emisión y absorción de los átomos, y la incapacidad de las teorías clásicas para explicarlos, lo que llevó a la formulación de la teoría cuántica en el siglo XX.
La observación de los espectros estelares tomó impulso en 1860 con Giovanni Battista Donati en Florencia y luego con Lewis M. Rutherfund en Nueva York, George Biddel Airy en Greenwich, William Huggins en Londres y Angelo Secchi en Roma.
En 1862 el astrónomo sueco Jonas Ångström aumentando la precisión de medida de la amplitud de banda identificó líneas de hidrógeno en el sol. La identificación del elemento hidrógeno ya había sido realizada en 1766 por el físico y químico inglés Cavendish
En 1868, el astrónomo inglés Norman Lockyer descubrió una línea inexplicada en el espectro del Sol que elidentificó como un nuevo elemento químico, el Helio.
Lockyer tiempo después fundó la revista Nature y fue su editor por 50 años. Independientemente de ello, el astrónomo francés Pierre-Jules-César Jansse también identificó esta línea durante el mismo año que Lockyer.
Solamente 27 años más tarde el elemento químico Helio fue descubierto en la Tierra por el químico Inglés William Ramsay, cuando el espectro de un mineral de uranio conteniendo helio produjo una línea en la posición exacta de aquella encontrada por Lockyer en el espectro del Sol.
Hoy día sabemos que el Helio es el segundo elemento más abundante en el Universo, solo precedido por el Hidrógeno. A través de la espectroscopía, los científicos pueden determinar la composición de estrellas distantes, galaxias e incluso nebulosas. Esto ha permitido a los astrofísicos entender mejor la evolución estelar y la formación de galaxias, proporcionando una visión más completa de nuestro Universo.