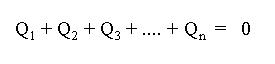Conceptos Básicos de Calorimetría
Las sensaciones de caliente o frío que sentimos en el cotidiano están relacionadas a los intercambios de energía entre nuestro cuerpo y el medio ambiente.
La sensación de caliente está relacionada a la ganancia de energía y la de frío a la pérdida de energía por nuestro cuerpo.
Esto sucede porque, al colocar dos cuerpos cualesquiera en contacto, la energía térmica fluye naturalmente del cuerpo más caliente al más frío.
La calorimetría es la parte de la Termología que estudia el calor y sus medidas.
UNIDADES DE MEDIDA
Caloría ( cal ), es la más utilizada.
Joule, la unidad oficial del Sistema Internacional de Unidades (S.I.)
Btu (Btu = unidad térmica del sistema británico)
1 Btu = 1055 Joules = 252 calorías
1 Caloría = 4,186 Joules
1 Caloría = 1 Kilocaloría = 1000 calorías = 4 186 Joules = 3,97 Btu
La caloría utilizada por médicos y nutricionistas es en realidad la Kilocaloría (Kcal), también llamada gran caloría. La unidad BTU continúa siendo utilizada en ingeniería, principalmente en la rama que toca la refrigeración (aparatos de aire acondicionado, cámaras de frio, etc).
Capacidad Térmica de un Cuerpo
La capacidad térmica de un cuerpo es la razón entre la cantidad de calor que el cuerpo intercambia (ganando o perdiendo) y la variación de temperatura que el sufre en este intercambio.
Su unidad de medida en el sistema internacional de unidades (S.I.) es el Joule/Kilocaloría, siendo que la más utilizada es la Caloría / oC.
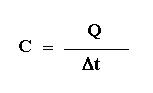
Calor específico de una sustancia (c)
Llamamos calor específico de una sustancia (c) a la razón entre la cantidad de calor que la sustancia intercambia y el producto entre su masa y la variación de temperatura sufrida.
Esta magnitud tiene su unidad de medida en el Sistema Internacional de Unidades (S.I.) y es el Joule/Kg, sin embargo la más utilizada es la Caloría/g. oC
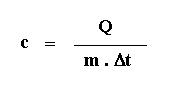
Calor específico de algunas sustancias
|
Sustancia |
en cal/g oC |
sustancia |
en cal/g oC |
|
Agua |
1,00 |
Hielo |
0,55 |
|
Aluminio |
0,22 |
Latón |
0,094 |
|
Arena |
0,20 |
Mercurio |
0,033 |
|
Cobre |
0,093 |
Oro |
0,032 |
|
Plomo |
0,031 |
Plata |
0,056 |
|
Estaño |
0,055 |
Vapor de agua |
0,48 |
|
Hierro |
0,11 |
Vidrio |
0,20 |
|
Éter |
0,56 |
Alcohol |
0,58 |
|
Acetona |
0,52 |
Cemento |
0,20 |
|
Etanol |
0,59 |
Metanol |
0,61 |
|
Silicio |
0,17 |
Titanio |
0,054 |
El cuerpo humano necesita de energía para su mantenimiento y para desempeñar tareas. La tabla a continuación muestra la energía absorbida por el organismo para cada 100 gramos de ciertos alimentos.
|
Alimentos |
Energía (en Kcal) |
Alimentos |
Energía (en Kcal) |
|
Lechuga |
15 |
Escarola |
20 |
|
Sandía |
30 |
Zanahoria |
40 |
|
Gaseosas |
40 (100 ml) |
Cerveza |
45 (100 ml) |
|
Naranjas |
50 |
Lenguado |
70 |
|
Papas/Patata |
80 |
Vino |
85 (100 ml) |
|
Banana |
90 |
Langosta |
90 |
|
Pollo |
200 |
Aguacate |
250 |
|
Pan |
270 |
Miel |
290 |
|
Frijoles |
340 |
Arroz |
260 |
|
Carne |
360 |
Bacalao |
380 |
|
Azúcar |
390 |
Chocolate |
470 |
|
Hígado |
136 |
Huevo |
163 |
|
Leche de vaca |
63 |
Arroz cocido |
167 |
Calor de Combustión
Todos los organismos humanos necesitan energía para sobrevivir. Los animales por ejemplo obtienen esa energía de la alimentación de forma primordial. El ser humano a través de la alimentación ingiere carbohidratos, proteínas y grasas que juntos posibilitan una provisión de energía necesaria para la realización de todas las actividades diarias.
Las máquinas y motores también necesitan energía para realizar trabajo, en estos casos, la principal fuente de energía es el combustible. Los combustibles así como los alimentos, contienen energía que puede ser liberada y utilizada por otros mecanismos.
La energía contenida en los alimentos y en los combustibles puede ser medida por medio de la quema (combustión). La combustión es una reacción exotérmica (liberación de calor) de una sustancia con oxígeno
Así entonces, la quema de 1 gramo de una determinada sustancia libera una cantidad de calor, denominado calor de combustión.
Calor de combustión es la cantidad de calor liberada en la quema de 1 gramo de una sustancia, medida en calorías/gramo.
La tabla a continuación nos muestra los calores de combustión de algunos combustibles.
|
Combustible |
Calor de Combustión (cal/g) |
|
Gas Hidrógeno |
29000 |
|
Gas Natural |
11900 |
|
Gasolina |
11100 |
|
Diesel |
10900 |
|
Alcohol Etílico |
6400 |
|
Leña |
2800 a 4400 |
Ecuación Fundamental de la Calorimetría

La cantidad de calor Q es también conocida como Calor Sensible
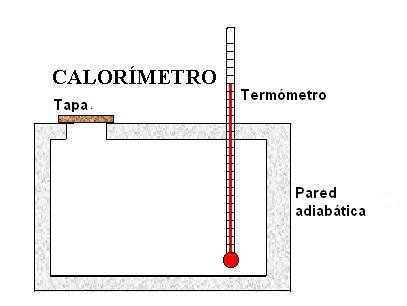
Calorímetro
El calorímetro es un aparato utilizado en laboratorios con el objetico de realizar experiencias que involucran intercambios de calor entre los cuerpos o sustancias.
Intercambios de Calor
Dos cuerpos o más (con temperaturas diferentes) cuando colocados en contacto (o próximos) pueden intercambiar calor entre si, obedeciendo la siguiente expresión: